Разделы статьи:
Биохимические подробности метаболизма Гомоцистеина весьма причудливы. Они уводят обычного клинициста в понимание глубокого смысла одноуглеродного обмена: от метилирования и мегалобластной анемии до дефектов развития нервной системы и депрессий. В этой статье мы спустимся на уровень молекул, чтобы разоблачить некоторые мифы, понять, почему дорогие витамины часто не работают, как дешевая фолиевая кислота обманывает гематологов, и почему некоторые генетические поломки можно просто игнорировать. Перед прочтением крайне рекомендую ознакомится с азами, которые я дал в предыдущей публикации: Гомоцистеин. История одного биомаркера.
Пути биотрансформации. Мы все знаем.
Статья задумывалась для «продвинутых пациентов», которые хотят глубоко понимать элементы метаболизма Гомоцистеина, но по факту будет полезна и врачам, которым нужна четкая, железобетонная аргументация, почему надо смотреть на HoloTC, MMA, В2 и почки, а не просто лечить бланк анализа.
Давайте начнем с самого простого, в фокусе — Гомоцистеин. Какие потенциальные пути дальнейшего превращения у него есть? Перечислю все, многие описал в предыдущей статье:
1) Реметилирование обратно в Метионин.
Это — официальный маршрут. Гомоцистеину возвращают метильную группу (с помощью В12/Фолата или Бетаина), и он снова становится полезным Метионином.
2) Трассульфурация в Цистеин и Глутатион.
Путь вниз. Организм с помощью витамина В6 делает из Гомоцистеина сильнейшую антиоксидантную защиту, точно пригодится.
3) Прямая экскреция почками.
Физиологический сброс. Почки — это не просто фильтр. Это гигантский завод по утилизации Гомоцистеина. Клетки почек захватывают его из крови. Часть они перерабатывают сами (у них очень мощная бетаиновая трасса), а излишки — просто сбрасывают в мочу. Именно поэтому, когда снижается СКФ при гипертонии, диабете или возрасте, аварийный клапан закрывается, и Гомоцистеин мгновенно повышается.
4) Циклизация Гомоцистеина в Тиолактон.
А вот здесь начинается настоящий детектив, с которого я и хочу начать. Что происходит, когда пути 1, 2 и 3 перегружены или сломаны? Гомоцистеина в клетке становится слишком много.
Тиолактоны и Гомоцистин
Ничто в мире не работает идеально гладко, без ошибок, включая биохимические реакции в организме. Но у нас есть внимательные системы контроля качества: если что-то пошло не так, продукт выбраковывается. Когда, в силу разных причин, Гомоцистеина становится много происходит роковая ошибка. Гомоцистеин по своей структуре безумно похож на Метионин (ведь это просто «раздетый» Метионин). И когда клетка начинает строить новые белки, ее сборочный аппарат (фермент метионил-тРНК-синтетаза) в спешке ошибается: он хватает Гомоцистеин вместо Метионина и пытается встроить его в белок!
В норме метионил-тРНК-синтетаза (биохимики называют ее MetRS) садит Метионин на транспортную РНК и отправляет в цех сборки белка. Если нужен Метионин для аминокислотной последовательности новой молекулы белка – пожалуйста, вот он. Но тут на тРНК она садит Гомоцистеин. В последний момент система контроля качества (редакторский центр фермента) замечает подмену: «Стоп, это не метионин!». Фермент выплевывает бракованную молекулу. Но в процессе этого жесткого «выплевывания» молекула Гомоцистеина скручивается в кольцо.
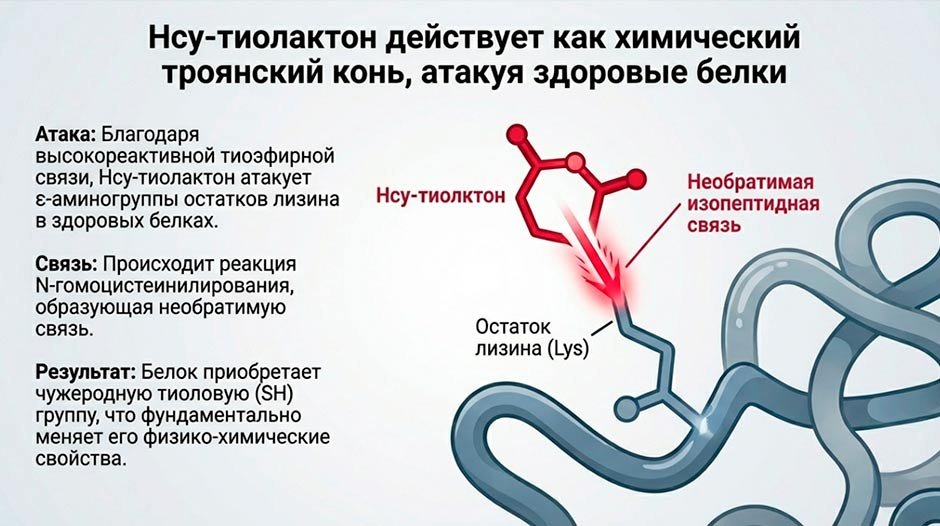
Так рождается Гомоцистеин-Тиолактон (далее -HTL или просто Тиолактон).
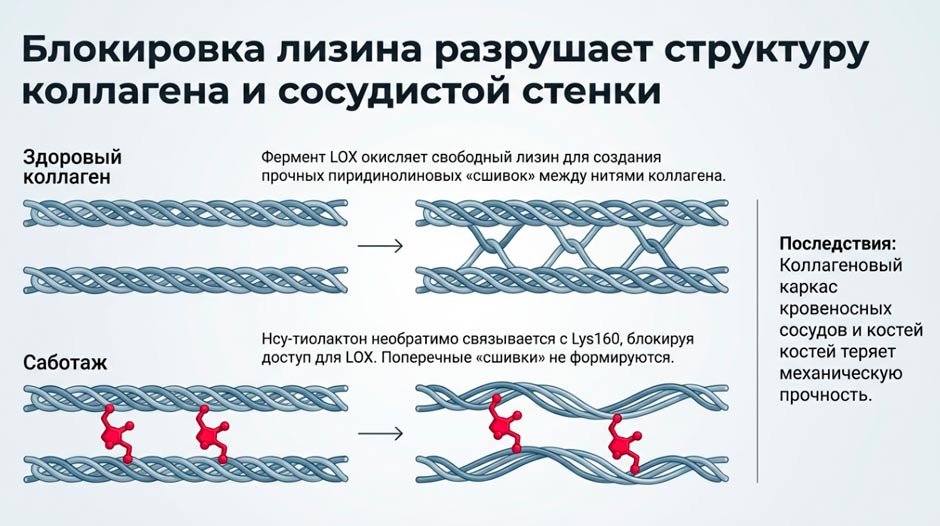
И вот этот Тиолактон — настоящий химический террорист. В отличие от обычного Гомоцистеина, тиолактон химически суперагрессивен. Он вырывается в кровь и начинает намертво прилипать к нормальным белкам нашего тела, предпочитая Лизин стенок сосудов (этот процесс называется N-Гомоцистеинилирование). Эндотелий теряет свою структуру. Иммунная система организма видит эти изуродованные тиолактоном белки, принимает их за чужаков и начинает атаковать собственные сосуды! Происходит воспаление и повреждение сосудистой стенки.
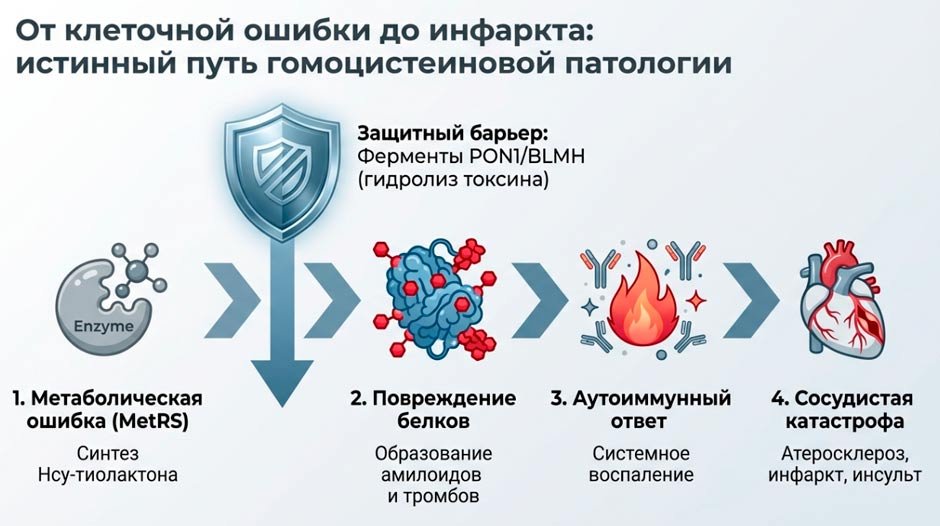
Пока Гомоцистеин находится в пределах 10–15 мкмоль/л, организм справляется путями 1, 2 и 3. Тиолактона образуется ничтожно мало. Но когда Гомоцистеин переваливает за 30, 50 или 100 мкмоль/л, официальные пути захлебываются. Включается путь №4. В кровь выбрасываются большие дозы токсичного Тиолактона, который, как скальпель повреждает сосуды изнутри и провоцирует массивные тромбозы.
То, что это действительно так, и Тиолактон форма Гомоцистеина токсична подтверждает тот факт, что организм имеет встроенную защиту от него: ферменты детоксикации HTL – не буду расшифровывать, поверьте на слово это ферменты PON1, BLMH, BPHL. Если есть отдельные системы детокса, значит продукт не просто возникает, он реально вреден. Более того, в биохимическом смысле HTL способен N-Гомоцистеинилировать apoB-100 (по лизинам), а модифицированный таким образом «плохой холестерин» ЛПНП в экспериментах показывает более атерогенное поведение. Один из ключевых защитников против этой суперагрессивной субстанции — фермент PON1. Вы не поверите, но это ключевой игрок ЛПВП… Только за это ЛПВП можно назвать «хорошим», но правильнее — жизнеспасающим. У мышей с нокаутом гена PON1 воздействие Тиолактона вызывает тяжелые судороги и наблюдается высокая смертность из-за неконтролируемого повреждения белков.
Сегодня, Тиолактон – это то, что рассматривается в первую очередь, как повреждающее действие Гомоцистеина. Но не единственное. Все дело в том, что образующийся Гомоцистеин буферизируется альбумином. И до концентрации 50-60 мкмоль/л альбумин продолжает его удачно прикреплять на себя. А вот после этой цифры доступного альбумина больше нет. Гомоцистеин начинает поступать в кровь в виде свободной молекулы. 2 свободные молекулы Гомоцистеина спокойно объединяются в пару через дисульфидную связь, образуя дисульфидную форму Гомоцистеина (Гомоцистин) и смешанные сульфиды (преимущественно Гомоцистеин – Цистеин). Вот так выглядит сама буферизация альбумином и дисульфидные молекулы, где HCY – это Гомоцистеин:
Исторически именно дисульфидная химия с другими аминокислотами и между собой (Гомоцистин в первую очередь) тоже рассматривалась как повреждающая для эндотелия/коагуляции — это не исчезло, просто сейчас больше внимания уходит на HTL-ветку, как на очень конкретный реактивный метаболит. Но надо понимать, что этот вариант токсичности потенциально актуален при переполнении буфера альбумина.
И тут уместен вопрос – а при каких концентрациях Гомоцистеина, образование Тиолактона/Гомоцистина становится значимым и существенно влияет на сосуды и коагуляцию? Постараюсь ответить максимально корректно в медицинском плане и это ОЧЕНЬ важно, поскольку мы фактически сейчас говорим о токсичности Гомоцистеина, которая в его контексте и поддерживает огонь интереса к этой теме.
- 1
Порогов в стиле концентрации ЛПНП, с которого Тиолактон становится клинически значимым нет, потому что HTL — это не альтернативный путь утилизации, а побочный продукт производства, который присутствует всегда, но его количество и последствия растут по мере увеличения цифры гиперГомоцистеинемии.
- 2
Что известно точно: Тиолактон повышен при высоких цифрах Гомоцистеина (в т.ч. при дефектах CBS/MTHFR), и это считается одним из путей токсичности через N-homocysteinylation белков. Сильные клинические фенотипы тромбозов — это в первую очередь тяжёлая гиперГомоцистеинемия (наследственные формы), где Гомоцистеин часто >100 мкмоль/л и может быть очень высоким (в описаниях гомоцистинурии встречаются сотни мкмоль/л).
- 3
Нельзя сказать, что например, порог Тиолактон токсичности 30 мкмоль/л, таких данных просто нет, но разумная клиническая рамка все же, на мой взгляд, выглядит так:
Если Гомоцистеин 15–30: Тиолактон, конечно, образуется, но говорить «вот здесь именно он уже значимо повреждает сосуды/началась коагуляция» — преждевременно, не клинический факт и не наблюдается.
Если Гомоцистеин 30–50: вероятность выше, но все же это зона смешения причин внешнего характера, а не только Тиолактон (ХБП/дефициты/гипотиреоз и т.д.).
Если Гомоцистеин 50–100 при наличии тромбозной клиники или Гомоцистеин > 100 уже разумно думать, что и HTL-ветка, и другие реактивные формы будут существенно выражены и серьезно влиять на прогноз (клиническая тактика должна быть агрессивной).
На этом я закончу с описанием прямой токсичности Гомоцистеина, думаю тему раскрыл, а то все говорят – он такой плохой – а чем он плох/когда он плох никто не знает… Напомню, что в большинстве случаев мягкой гиперГомоцистеинемии (15-30 мкмоль/л) – это маркер дефицитов и иных процессов, а не токсичности per se.
Идем дальше, обещал же лайфхаки. Процесс реметилирования Гомоцистеина, давайте рассмотрим его под микроскопом.
Особенности реметилирования, у Гомоцистеина всегда есть план «Б»
Чтобы окончательно понять, почему уровень Гомоцистеина у двух людей с одинаковыми дефицитами может кардинально отличаться, нам нужно посмотреть на карту реметилирования (возврата Гомоцистеина обратно в Метионин). Оказывается, природа предусмотрела для этого не один, а целых два маршрута.
Маршрут №1. «Классическая магистраль» (Фолат + B12)
Это основной путь, который работает в большинстве клеток нашего тела. Здесь Гомоцистеину возвращают утерянную метильную группу, его попросту снова одевают и он превращается в Метионин. В этом процессе важно понимать жесткое разделение ролей:
- Фолат (в активной форме 5-MTHF) — это донор. Именно он приносит метильную группу.
- Витамин B12 (и зависящий от него фермент метионин-синтаза) — это переносчик.
И вот тут кроется важнейший клинический нюанс. Фолат и B12 делают общее дело, но если у человека дефицит именно B12, фолат не спасет ситуацию. Грубо говоря, на складе может быть полно груза (фолата), но если нет курьера (B12), груз никуда не поедет.
Маршрут №2. «Запасная объездная» (Бетаин/Холин)
А что делать, если на главной магистрали пробка, а возвращать (реметилировать) надо? Природа создала обходной путь, который работает в основном в печени и почках. На этой трассе метильную группу отдает совершенно другое вещество — Бетаин (производное холина), а руководит процессом фермент BHMT. Здесь вообще не нужны ни B12, ни фолаты! Организм использует эту объездную дорогу, чтобы компенсировать провалы на основном маршруте.
Именно поэтому Гомоцистеин — это не индикатор нехватки одного конкретного винтика. Это маркер суммарной нагрузки на систему. У одного пациента барахлит маршрут №1 (дефицит B12), у другого пуст маршрут №2 (проблемы с печенью и нехватка холина), у третьего снижена функция почек, и Гомоцистеин не выводится вообще. Более того – даже подробности классического процесса реметилирования могут влиять на Гомоцистеин с разных сторон, и я вот о чем:
Прецизионное описание реметилирования в фолатном цикле
Задача: преобразовать Гомоцистеин обратно в Метионин. Для этого к Гомоцистеину достаточно присоединить метильную группу и … все! Одетый в метильную группу Гомоцистеин = Метионин. Как это делает организм, поэтапно:
Этап №1.
Чтобы понять, как работает «классическая магистраль» реметилирования, нужно избавиться от одной частой иллюзии. Многие думают, что молекула фолиевой кислоты (витамина B9) сама по себе и есть тот самый спасительный донор метильной группы. Ничего подобного. Фолиевая кислота/фолаты из еды или таблеток — это «пустая тара». Это просто платформа, на которую еще нужно погрузить метильную группу.
Главным донором этого химического «навеса» (метильной группы) выступает другая аминокислота — Серин. Именно серин подплывает к фолату и жертвует ему углеродный атом. В этот момент образуется промежуточная конструкция с зубодробительным названием — 5,10-метилентетрагидрофолат (5,10-methylene-THF). Но чтобы эта конструкция с уже прицепленным дополнительным атомом углерода стала реально активной и готовой передать Гомоцистеину метильную группу, она должна пройти финальную стадию упаковки/активации.
Этап №2.
И вот тут на сцену выходит наш знаменитый фермент MTHFR. Его полное, академическое имя — метилентетрагидрофолатредуктаза. Инструкция по сборке этого фермента записана в гене, который надежно «прописан» в 1-й хромосоме. Задача фермента MTHFR проста, но критически важна: он берет промежуточную форму фолата и производит необратимую химическую реакцию (редукцию). Он буквально намертво защелкивает замок на этом углеродном грузе, превращая его в полноценную метильную группу. Всё! Молекула навсегда изменила свой статус. Теперь это 5-MTHF (5-метилтетрагидрофолат или в народе просто Метилфолат). Это активный, заряженный донор, готовый передать метильную группу Гомоцистеину. Но активный фолат не может просто бросить метильную группу в Гомоцистеин. Ему нужен посредник. И здесь начинается самая драматичная история в нашей биохимии.
Этап №3 или Ловушка фолатов: как витамин B9 обманывает гематологов
Передать метильную группу от активного фолата (5-MTHF) к Гомоцистеину может только один-единственный переносчик в организме — витамин B12 (кобаламин), работающий в составе фермента метионин-синтазы. Если витамина В12 достаточно, то метионин-синтаза легко перебрасывает метильную группу от активного Метилфолата на Гомоцистеин и образуется снова Метионин.
Но что происходит, если у человека жесткий дефицит B12?
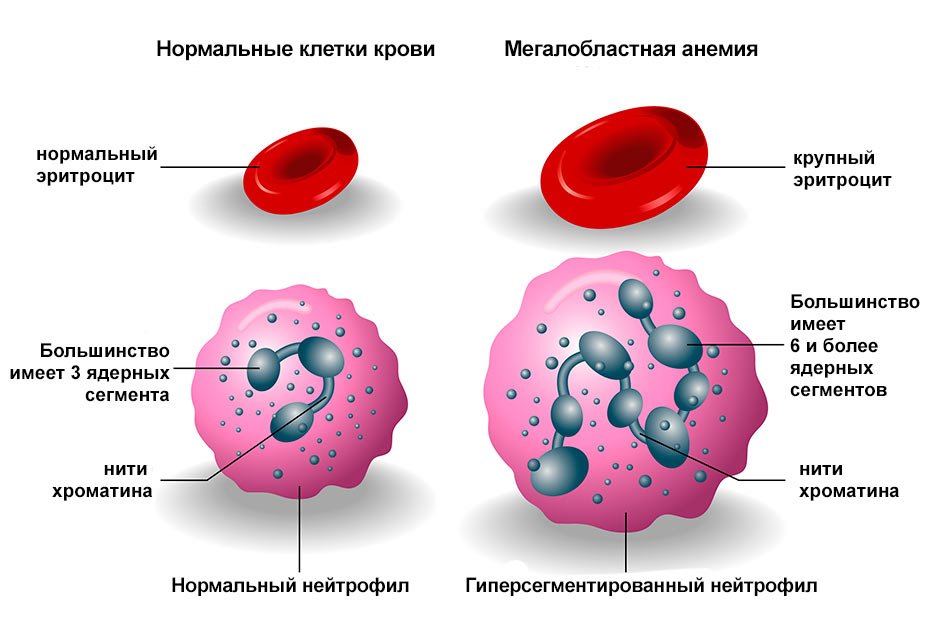
Активный фолат (5-MTHF) со своей метильной группой подъезжает к Гомоцистеину, но… переносчика нет. Реакция останавливается. В биохимии это называется «метил-фолатная ловушка» (methyl-folate trap). Фолат оказывается намертво заперт в своей активной форме с метильной группой наперевес, его много, но организм не может использовать ни его по прямому назначению, ни освободить фолат (!) из этой активной формы для других нужд. Начнет развиваться мегалобластная анемия (фолиево-В12) и тонкость этого процесса я хочу, чтобы читатели понимали.
Помните на Этапе №1 образовалась промежуточная, еще неактивная форма фолата с присоединенным атомом углерода. Казалось – ну зачем создавать нечто промежуточное? Присоедините метильную группу от Серина и сразу ее активируйте. Но тут дело вот в чем. Это промежуточное звено с труднопроизносимым названием в реальности — «свободный агент», который стоит на развилке. Если в клетке сейчас нет избытка Гомоцистеина, но зато клетка собирается делиться (например, это клетка крови, кожи или слизистой кишечника), этот агент отправляется не к ферменту MTHFR, а прямиком в цех сборки ДНК. Что он там делает? Как мы знаем из школы, генетический код ДНК — это длинный текст, написанный всего четырьмя буквами-нуклеотидами: А, Т, Г, Ц (Аденин, Тимин, Гуанин, Цитозин).
Так вот, чтобы напечатать букву «Т» (Тимин), организму нужна химическая заготовка и ровно один дополнительный атом углерода. Наш 5,10-метилентетрагидрофолат работает как уникальный художник, который может рисовать только… нет-нет не квадрат Малевича – а букву Т. Он подъезжает к конвейеру сборки ДНК и щедро отдает свой углеродный груз ферменту (тимидилатсинтазе). Бац! — и фермент «штампует» новенькую букву «Т».
Без этого промежуточного фолата синтез буквы «Т» физически невозможен. А нет буквы «Т» — текст ДНК написать нельзя. Клетка не может скопировать свои гены, ее деление останавливается. Именно поэтому, когда беременным не хватает фолиевой кислоты, у плода не могут нормально делиться клетки нервной трубки (возникают тяжелейшие пороки развития). И именно поэтому при дефиците витамина B9 у взрослых перестают делиться эритроциты в костном мозге, что приводит к той самой мегалобластной анемии. Вернемся в наш цикл реметилирования – образовался активный Метилфолат, а витамина В12 нет. Почему это называется «метил-фолатная ловушка» ?
Потому что система организма видит накапливающийся Гомоцистеин, и направляют все бОльшую долю неактивного фолата в процесс метилирования (активировать), чтобы снизить уровень Гомоцистеина. Но он там просто стоит без дела! Он не может отдать метил… При этом надо понимать, что после удачного метилирования наш активный Метилфолат превращается снова в… фолатную заготовку, которую можно использовать в синтезе ДНК! Но все фолаты оказываются заперты: скапливаются в метилированной форме и для синтеза ДНК наступает голод. Развивается анемия…
И вот тут интересная деталь: можно дать человеку массированную дозу фолатов и… ситуация по гематологии подкрасится — дело в том, что гигантские дозы неметилированной фолиевой кислоты создают в клетке эффект прорванной плотины (массовое действие субстрата). Эта лавина сырья находит обходные пути. Часть фолата успевает пойти на синтез ДНК до того, как фермент MTHFR запрет его в метильную ловушку.
Синтез ДНК разблокируется! Эритроциты начинают радостно делиться, анемия исчезает, пациент розовеет, а врач-гематолог облегченно выдыхает, глядя на идеальный общий анализ крови.
Но есть одна катастрофическая проблема. Витамина B12 по-прежнему нет. А без B12 невозможен не только перенос метильной группы на Гомоцистеин, но и синтез миелина — защитной оболочки наших нервов. Пока мы радовались красивому анализу крови, нервная система пациента продолжала молча и безвозвратно разрушаться. Фолиевая кислота просто надела маску благополучия на истинную причину катастрофы.
Сейчас самое время задать вопрос – а что так трудно взять анализ на В12? (именно пару фолиевая кислота и В12 берут при мегалобластной анемии). Ответ: не трудно, только в большинстве случаев – это гадание на «кофейной гуще», в большинстве случаев мы получим норму при истинном дефиците, надо конечно брать анализ на голотранскобаламин или HoloTC.
Во всей этой истории с реметилированием по фолатному циклу есть еще 2 важные детали, которыми я хочу также поделиться. Первая — территорию самой великой путаницы в современной медицине.
Генетика (MTHFR) и главная биохимическая иллюзия
Если вы хоть раз интересовались темой витаминов или биохакинга, вы наверняка слышали аббревиатуру MTHFR. Да, тот самый MTHFR, который мы только что разбирали на 2 этапе: он активирует промежуточную форму фолата. Сегодня анализ на мутации в этом гене продается как «генетическая причина всех бед с Гомоцистеином» и повод пожизненно пить дорогие метилированные формы витаминов. Давайте разберемся.
Логика врача может выглядеть железобетонно:
- Фермент MTHFR делает ту самую активную форму фолата (5-MTHF), которая нужна для классической магистрали.
- Если в гене MTHFR есть «поломка», активного фолата мало → реметилирование останавливается → Гомоцистеин растет.
- Раз Гомоцистеин связан с инфарктами и инсультами, значит, ген MTHFR — это ваш личный генетический приговор сосудам!
Звучит страшно? Да. Продается отлично? Еще бы. Но в реальности эта цепочка работает совсем иначе. Вся проблема в том, что люди путают два абсолютно разных генетических мира.
Действительно, существуют тяжелые мутации, при которых фермент MTHFR выключен почти полностью. Это серьезные заболевания, которые проявляются еще в детстве тяжелейшими сосудистыми и неврологическими нарушениями. Там уровень Гомоцистеина зашкаливает, и обычные витамины не работают. Но это — редчайшие случаи, требующие сложного лечения. И это не та история, которую массово находят в генетических исследованиях по Гомоцистеину! Если MTHFR будет полностью выключен вы узнаете об этом в раннем детстве… И с нехорошей стороны узнаете. Но если вы ничего не замечали до 2 лет, то это не оно.
То, что называют «мутацией MTHFR» в популярных тестах — это полиморфизм. Ген не сломан! Фермент просто работает чуть медленнее. Грубо — труба стала чуть-чуть уже. Если давление воды в системе высокое (у вас достаточное потребление фолатов с пищей, большой фолатный пул), то через эту слегка зауженную трубу пролетит ровно столько фолата, сколько нужно организму. Вы даже не заметите этой генетической особенности! И встречаемость их в популяции … частая!
Генотип начинает проявлять себя (и Гомоцистеин ползет вверх) только тогда, когда накладывается дефицит. Если вы не едите зелень, у вас проблемы с кишечником, воспаление или снижена функция почек — вот тогда «ленивый» фермент MTHFR усугубит ситуацию. Именно поэтому современная медицина говорит: мы лечим не ген, мы лечим фенотип и контекст.
Повышенный Гомоцистеин определяется не одной буквой в ДНК, а балансом: сколько фолата мы получаем + как работает звено B12 + спасает ли нас запасная бетаиновая трасса + в каком состоянии почки. Один и тот же вариант гена MTHFR может никак не проявляться у человека со здоровыми почками и хорошим питанием, но стать проблемой при жестком дефиците. Я даже памятку составил по этим вопросам:
Миф 1: «У меня мутация MTHFR, мне нельзя обычную фолиевую кислоту, только дорогой метилфолат».
Факт: В абсолютном большинстве случаев решает объем фолатного пула (достаток витамина B9 в целом) и отсутствие дефицита B12. Форма витамина имеет лишь вторичное значение, если нет специфических медицинских показаний. Увеличение субстрата ВСЕГДА компенсирует медленную работу фермента.
Миф 2: «Полиморфизм MTHFR — это высокий риск инфаркта».
Факт: Влияние этого гена на реальные сердечно-сосудистые катастрофы (если оно вообще есть) ничтожно мало по сравнению с настоящими убийцами: курением, высоким «плохим» холестерином (ЛПНП/ApoB), гипертонией, диабетом и снижением функции почек, забудьте.
Миф 3: «Ген MTHFR нужно лечить пожизненно».
Факт: Гены не лечат. Лечат реальные причины: закрывают дефициты фолатов и B12, компенсируют гипотиреоз, следят за здоровьем почек и снимают системное воспаление. И да – это нестрашно, полиморфизмы MTHFR — обычная популяционная «норма», которая встречается почти у каждого второго… (это правда)
А вот какие полиморфизмы известны и что определяют в лабораториях?
В быту под «мутациями MTHFR» обычно имеют в виду очень частые полиморфизмы (варианты) гена:
- C677T (rs1801133)
- A1298C (rs1801131)
Вариант C677T — наиболее «жёсткий» по активности фермента.
- CT (гетерозигота): активность MTHFR примерно ~60–67% от нормы
- TT (гомозигота): активность примерно ~25–30% от нормы
Но даже при мутации ТТ чаще наблюдают рост гомоцистеина в условиях недостатка фолата/рибофлавина (B2) и при сопутствующих факторах (B12-дефицит, ХБП и т.п.). Еще раз — сам по себе генотип не является диагнозом — важен фенотип!
Вариант A1298C — обычно мягче. Этот вариант в среднем снижает активность еще меньше:
- AC: сохраняется активность около ~83%
- CC: около ~61%
Обычно A1298C не даёт выраженную гипергомоцистеинемию в одиночку.
Может возникнуть резонный вопрос: если вдруг есть полная блокада MTHFR (повторю – это крайне редкая патология), то почему ее нельзя лечить Метилфолатом, тем самым активным 5-MTHF? Гениальный вопрос. Если у человека редкая, тяжелейшая генетическая поломка MTHFR (фермента вообще нет), почему нельзя просто дать ему готовую таблетку метилфолата (5-MTHF), обойти поломанный ген и решить проблему?
Ответ кроется в суровой анатомии и физиологии:
- Гематоэнцефалический барьер. Тяжелый дефицит MTHFR бьет в первую очередь по мозгу (тяжелые неврологические нарушения у детей). Чтобы мозг получил метилфолат, витамин должен пройти через рецепторы гематоэнцефалического барьера (в реальности не совсем ГЭБ, а барьер кровь–ликвор на уровне сосудистого сплетения, но сейчас это не так важно). Когда мы пьем метилфолат в таблетках, он отлично плавает в крови, но пропихнуть его в мозг в нужных, гигантских терапевтических концентрациях через рецептор (FRα) просто невозможно.
- Эффект переполненного бассейна. При тяжелой генетической поломке уровень Гомоцистеина в крови зашкаливает так сильно, что одного метилфолата физически не хватит, чтобы разгрести эти завалы.
Поэтому врачам при тяжелых мутациях приходится действовать хитрее: они искусственно «разгоняют» запасную бетаиновую трассу (назначая огромные дозы бетаина), чтобы печень/почки взяли на себя удар и выкачала этот токсичный объем Гомоцистеина из крови. Вот почему безвитаминная маршрутизация по плану «Б» реметилирования так важна. Бетаин – как донор метильной группы – просто палочка-выручалочка в таких ситуациях!
Некоторые детали: вопрос-ответ
- Мясоед (Нагрузка сырьем)
Как мы помним с самого начала статьи, Гомоцистеин получается из Метионина. А где больше всего Метионина? В красном мясе! Человек, который ест много животного белка, ежедневно отправляет на нашу «биохимическую станцию переработки» огромные партии сырья. Конвейер работает активно, Гомоцистеина образуется много. Это не патология, это просто отражение диеты: больше груза на входе — чуть больше промежуточных молекул в моменте.
Вопрос: как организм понимает, что надо меньше реметиллировать (Метионина много!), а начать больше сбрасывать в транссульфурацию?
Ответ: в клетке встроен гениальный механизм обратной связи. И пультом управления здесь выступает молекулаSAM(S-аденозилМетионин — та самая активная форма Метионина, готовая отдавать метильные группы, она же аптечный «Гептрал»). Когда клетка сыта, уровень SAM начинает расти. SAM циркулирует по цитозолю и действует как регулятор, выполняя 2 действия:
SAM подходит к ферменту MTHFR (нашему защелкивателю) и… выключает его (аллостерическое ингибирование). MTHFR перестает делать метилфолат. Переработка Гомоцистеина по пути назад (в Метионин) мгновенно тормозится. Типа: «Хватит производить Метионин, у нас его и так девать некуда!»
Одновременно с этим SAM идет к другому ферменту — CBS (тому самому, который работает с витамином B6 и переводит Гомоцистеин вниз, в цистеин и глутатион). SAM его активирует! Типа SAM говорит: «Раз у нас избыток сырья, открывай дренаж, пускай Гомоцистеин на производство антиоксидантов (глутатиона) — в хозяйстве пригодится!»
- Мужчина (Мышцы и синтез креатина)
Вопрос: куда идут метильные группы в процессе метилирования SAM- ом?
Ответ: почти 70% всех метильных групп в нашем организме тратится на одну-единственную задачу — синтез креатина (энергии для сокращения мышц). У мужчин мышц больше, креатина им нужно больше. Значит, активный Метионин (SAM) безостановочно отдает метильные группы на нужды мускулатуры. А мы помним формулу: отдал метил = превратился в Гомоцистеин. Чем больше мышц и чем активнее они работают, тем выше базовый уровень Гомоцистеина.
- Кофеин (Доказанный триггер)
Вопрос: кофе повышает уровень Гомоцистеина?
Ответ: это малоизвестный, но научно доказанный факт: большое количество кофе (от 3-4 чашек в день, особенно нефильтрованного, вроде эспрессо или в турке) достоверно повышает уровень Гомоцистеина.
Во-первых, кофеин работает как легкое мочегонное, ускоряя выведение водорастворимых витаминов (тех самых B6, B9, B12). Во-вторых, вещества в кофе (хлорогеновая кислота) создают дополнительную нагрузку на печень, оттягивая на себя ресурсы метилирования. Любовь к крепкому кофе стабильно «накидывает» к анализу 2 единицы.
Лайфхак вместо послесловия:
Призрак витамина B2 (Рибофлавина)- Серый кардинал фолатного цикла.
На приеме пациентка с чуть повышенным уровнем Гомоцистеина, и ее это беспокоит. Она сделала все! Отрегулировала все витамины, применила их самые современные формы и методы ввода, ну ничего нет, кроме… гипофункции щитовидной железы в анамнезе. И эту гипофункцию скорректировала! А Гомоцистеин повышен.
Мы привыкли думать, что главным героем возврата Гомоцистеина в Метионин является фолат, а главным ферментом — наш любимый MTHFR. Но есть один нюанс, о котором забывают 90% врачей. Чтобы фермент MTHFR вообще включился и смог защелкнуть метильную группу на фолате (превратив его в активный 5-MTHF), ему нужен двигатель. Машина MTHFR просто так не поедет! И этим двигателем является молекула FAD (флавинадениндинуклеотид).
А из чего организм делает этот FAD? Исключительно из витамина B2 (рибофлавина)! Именно поэтому рибофлавин — это серый кардинал фолатного цикла. Нет рибофлавина — двигатель глохнет, фермент MTHFR останавливается (даже если с генетикой у вас всё идеально), фолат не становится активным, и Гомоцистеин ползет вверх. Почему никто не задает вопрос про витамин В2? – да потому что обычно его завались в питании и почти никогда не наблюдается его дефицита. Более того – в крови его не определить, а дефицит наблюдается только по заедам у краев губ, шелушению кожи и небольшой усталости. И то – очень редко. Поэтому по умолчанию считается – с В2 все в порядке.
При чем здесь щитовидная железа?
А вот тут начинается настоящая медицинская магия. Чтобы превратить рибофлавин из еды (или обычной витаминки) в тот самый рабочий двигатель FAD, организму нужны гормоны щитовидной железы (тироксин). Если у человека гипотиреоз, этот процесс блокируется. У вас может быть идеальное питание, идеальная генетика и горы фолиевой кислоты в крови. Но из-за нехватки гормонов щитовидки витамин B2 не превращается в свою активную форму. Фермент MTHFR остается без энергии и засыпает. Конвейер встает, Гомоцистеин растет.
Более того, если у человека есть пресловутая мутация MTHFR (когда фермент генетически «ленивый» и работает вполсилы), именно высокие дозы рибофлавина (B2) способны «разогнать» этот ленивый фермент и компенсировать генетический дефект даже лучше, чем конские дозы дорогого метилфолата! Рибофлавин выступает как стабилизатор для хрупкой, мутантной структуры фермента, не давая ему развалиться в клетке. А она разваливается уже при температуре тела! Именно поэтому исследования показывают: у людей с мутацией MTHFR (а это от 40 до 50% населения) добавление простого, копеечного рибофлавина снижает Гомоцистеин великолепно! Но… продавать дорогой «активный метилфолат» за … денег в любой валюте маркетологам гораздо выгоднее, чем копеечный витамин B2 из ближайшей аптеки.
Но ведь гипотиреоз компенсировали! Да, если ТТГ в норме и Т4 свободный ему вторит, то формально это норма и цель достигнута, но клиническая норма в клетке будет только через пару месяцев. Так что…
Витамин B2 — это не панацея от всех видов высокого Гомоцистеина. Но это тот самый «серый кардинал», о котором обязан помнить грамотный врач, когда:
- Гомоцистеин высокий, а В12 и фолаты в крови идеальные.
- У пациента гипотиреоз ИЛИ
- У пациента генетически подтвержденный полиморфизм фермента MTHFR.
Окончание
Все, закончил, а то меня не остановить. Там же еще транссульфурация с глутамином – а это вообще антиейджинг, отдельный мир. Надеюсь, – информация была познавательной.